Bonjour,
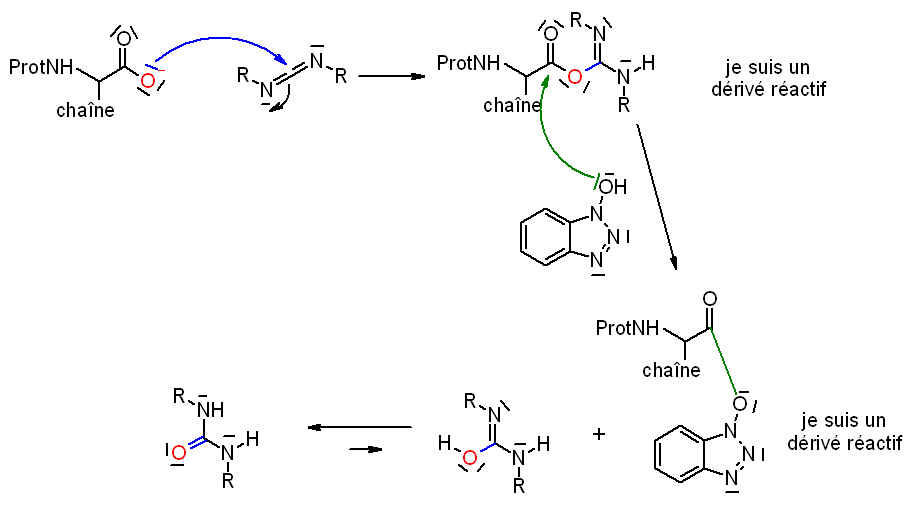
Je réalise un couplage peptidique au labo en utilisant HOBt (N-Hydroxybenzotriazole) et EDCI (1-(3-dimethylaminopropyl)-3-ethylcarboiimide), à 1.1 equivalents chacun, afin d'activer l'acide.
Cependant, en cherchant un peu on se rend compte que ces 2 molécules ont la même fonction, à savoir former un intermédiaire plus réactif que l'acide carboxylique. HOBt semble avoir l'avantage d'éviter la racémisation en alpha du groupement carbonyle alors que EDCI est un peu plus réactif.
Ma question est donc la suivante : pourquoi utilise t'on ces 2 molécules ensemble alors qu'elles ont la même action ? Ne serait il pas préférable d'utiliser uniquement HOBt ? D'autre part, j'ai vu que HOBt est généralement utilisé en quantité catalytique, alors, pourquoi me fait on utiliser 1.1 equivalent ?
Merci
-----