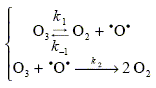Bonjour tout le monde,
j'ai un petit soucis concernant cette correction je vous ai remis l'ennoncé en entier.
Lair atmosphérique est un mélange de gaz dont les constituants essentiels sont le diazote et le dioxygène. À ces deux constituants sajoutent en quantités variables, mais faibles, dautres gaz dont lozone O3. Cet ozone forme une fine couche protectrice permettant de filtrer des rayonnements nocifs arrivant sur Terre.
Le but de cette partie est détudier le mécanisme de la décomposition de lozone, et linfluence des chlorofluorocarbures (C.F.C.) sur cette décomposition (qui mène au problème actuel du « trou » dans la couche dozone).
Lozone est thermodynamiquement instable par rapport au dioxygène. Il peut se décomposer, en labsence de catalyseur, suivant la réaction très lente :
2 O3(g)--> 3 O2(g)
pour laquelle on peut proposer le mécanisme suivant :
Déterminer la loi de vitesse de la réaction précédente en fonction de [O3], [O2] et des constantes de vitesse.
donc pour ça on utilise l'AEQS jusque là je suis d'accord mais dans le corrigé il est écrit ensuite ...
2 O3(g)--> 3 O2(g) ; v = 1/3 d[O2]/dt. ( je suis d'accord )
d[O2]/dt = k1[O3]-k-1[O2][.O.] + 2k2 [O3][.O.] <== là je ne suis pas d'accord O2 n'est pas un intermediaire reactionnel donc on ne peut pas lui appliquer l'AEQS ?? j'ai du mal comprendre si quelqu'un pouvait m'eclairer merci d'avance
-----