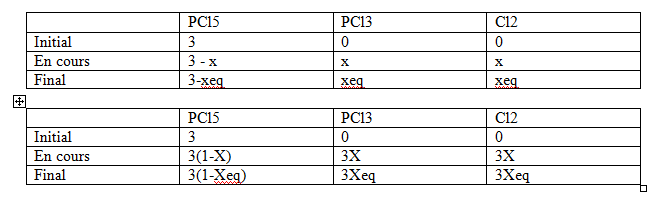
On étudie la réaction PCl5 <=> PCl3 + Cl2 à partir de 3 moles de PCl5, la pression initiale étant de 1 bar. Une fois l'équilibre établi, on mesure une pression égale à 1,25 bar (le volume étant maintenus constants.)
En déduire les évolutions de la réaction en utilisant l'avancement puis la conversion.
Alors :
http://image.noelshack.com/fichiers/...tachlorure.png
Mais à quel moment utilise-ton la pression ?
Merci d'avance !
-----