Bonjour,
Je n'arrive pas à dessiner les profils énergétiques de cette question :
(a) Pour une réaction hypothétique A f P, tracer deux graphiques représentant le profile énergétique (énergie libre en fonction des coordonnées de réaction) de la réaction (faire apparaître les états fondamentaux A et P et létat de transition) dans deux situations où les concentrations de A et de P à léquilibre sont identiques, mais où la vitesse de la réaction est différente. Expliquer et justifier brièvement votre réponse.
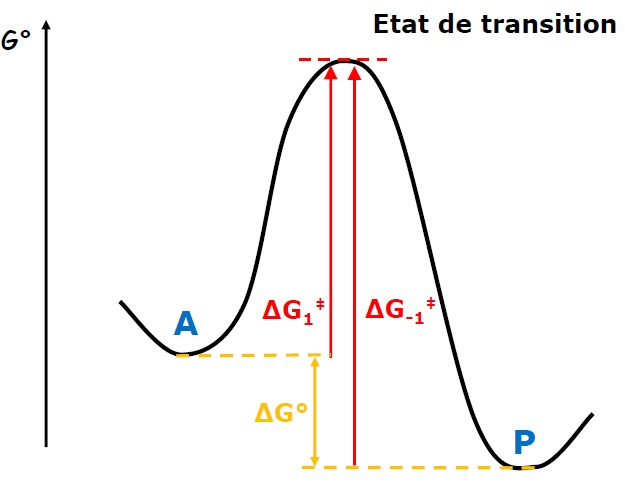
Je sais que le profil ressemble à celui ci dessous.
Et je sais que la vitesse des réactions dépend de la concentration du réactif
Du coup je ne comprend pas la difference que l'on va observer entre les 2 graphiques
Merci pour votre aide
-----




