Salut. Pour pouvoir interagir, deux orbitales (atomiques ou moléculaires) doivent posséder des énergies voisines et surtout, les mêmes propriétés de symétrie (d'après ce que je sais, mais vous me corrigerez si je me trompe).
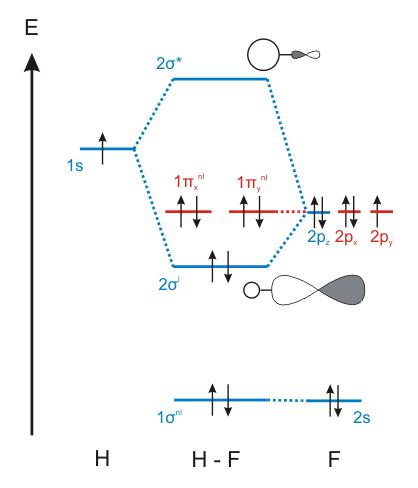
Mais comment se fait-il alors qu'on fasse intéragir des orbitales s et p parfois, comme dans ce diagramme orbitalaire H-F:
Les orbitales s et p n'ont pas les mêmes propriétés de symétrie! La première est anisotrope alors que la deuxième possède un plan d'antisymétrie.
Merci de bien mexpliquer ce qui cloche!
-----