Bonjour,
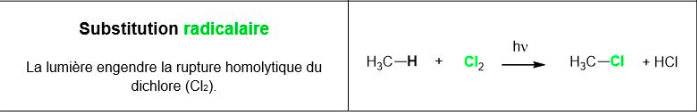
Dans cette réaction radicalaire lorsque on apporte une énergie hv (h*mu, je suppose), on a une réaction radicalaire entre H et Br. Mais je me demandais si cela n'est valable que pour les substitutions : dans mon cours en ce qui concerne, les additions pour faire une réaction radicalaire on utilise du peroxyde. Mais peut-on par exemple utiliser le peroxyde pour provoquer une réaction radicalaire servant à une substitution et utiliser l'énergie hv pour provoquer une réaction radicalaire servant à une addition ?
Merci d'avance
Cordialement
Pakaa
-----