Bonjour
J'ai un exercice où on me demande de déterminer les ordres partiels lors d'une substitution nucléophile (bromoéthane - soude).
j'ai vu qu'une question avait déjà été posée sur ce forum au sujet de ce même exercice (https://forums.futura-sciences.com/chimie/655511-chimie-organique-cinetique.html)
A partir de la réaction de dosage, j'en déduis la concentration restante en HO-, puis l'avancement x me permettant ainsi de remonter à la concentration en bromoéthane restante.
j'envisage une SN2, donc d'ordre partiel 1 par rapport à chacun des réactifs : je calcule donc le Ln de chaque concentration et la représentation graphique de Ln [réactif] en fonction du temps devrait être une droite de pente négative (-k).
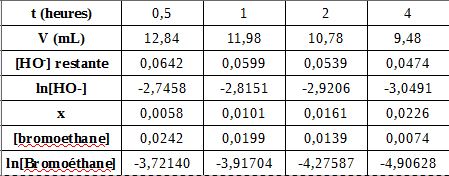
Mes résultats
Quand je modélise, je suis assez loin d'obtenir une droite (coefficient de corrélation de 0.97 pour l'ion hydroxyde, 0.998 pour le bromoéthane)
J'ai essayé l'ordre 2 qui ne donne pas plus de meilleurs résultats (plutôt logique pour le coup)
Ai-je fait une erreur dans mon raisonnement ou mes calculs ?
Merci pour votre aide
-----