Bonjour,
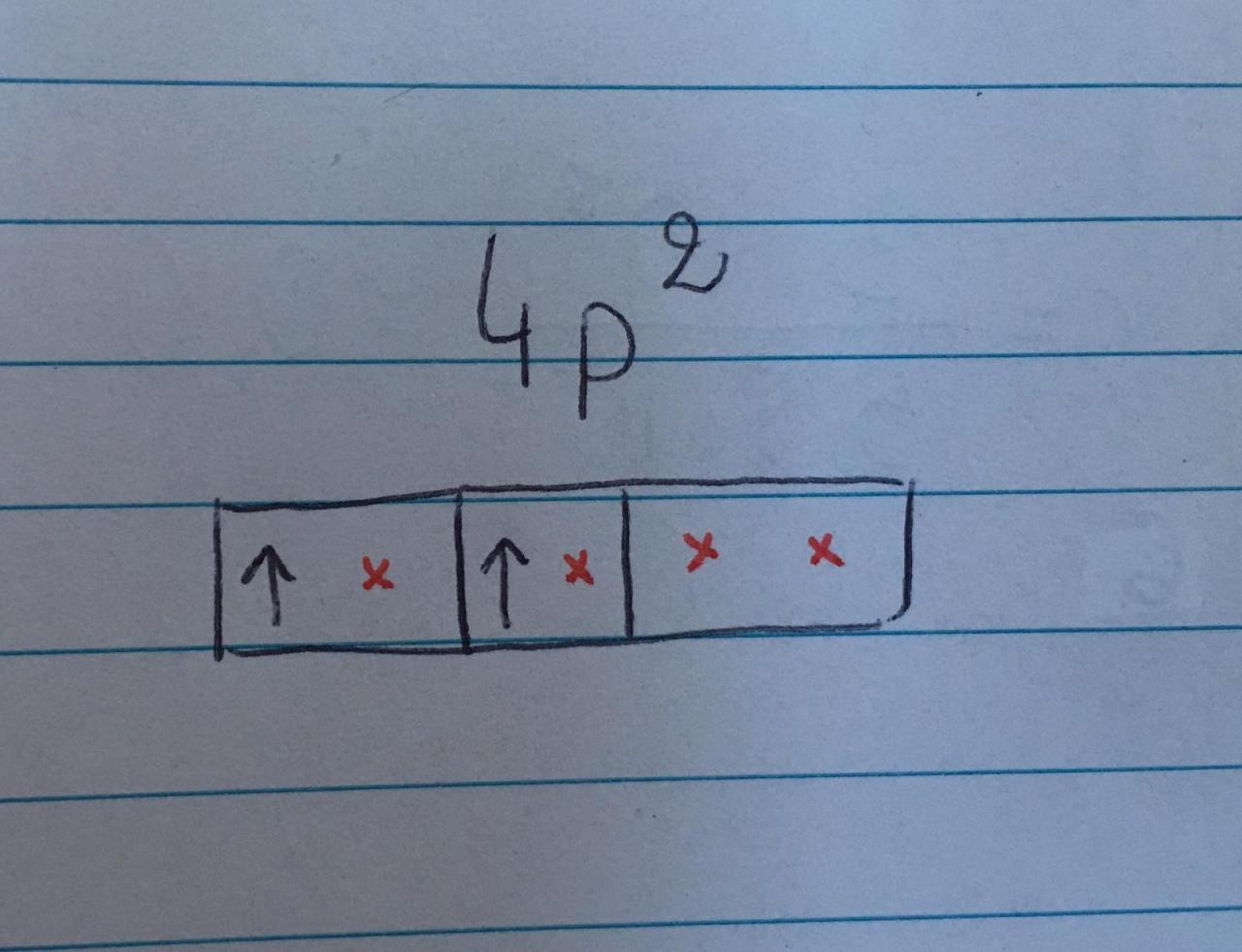
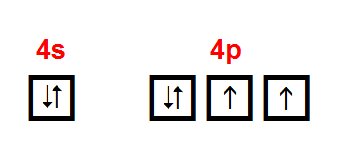
qu'est-ce qu'un électron périphérique non appariés, car dans cet exercice, ils disent à la proposition D. "A l'état fondamental, il possède 2 électrons périphériques non appariés"
Sauf la configuration étant (Ar) 4s2 3d10 4p2, j'aurai dis 4 éléctrons non appariés, je ne comprend pas trop la différence du coup et pourquoi la réponse est noté comme "vrai".
Documents scannés.pdf
-----