Bonjour pouvez-vous m'éclairer sur cet exercice s'il vous plaît ?
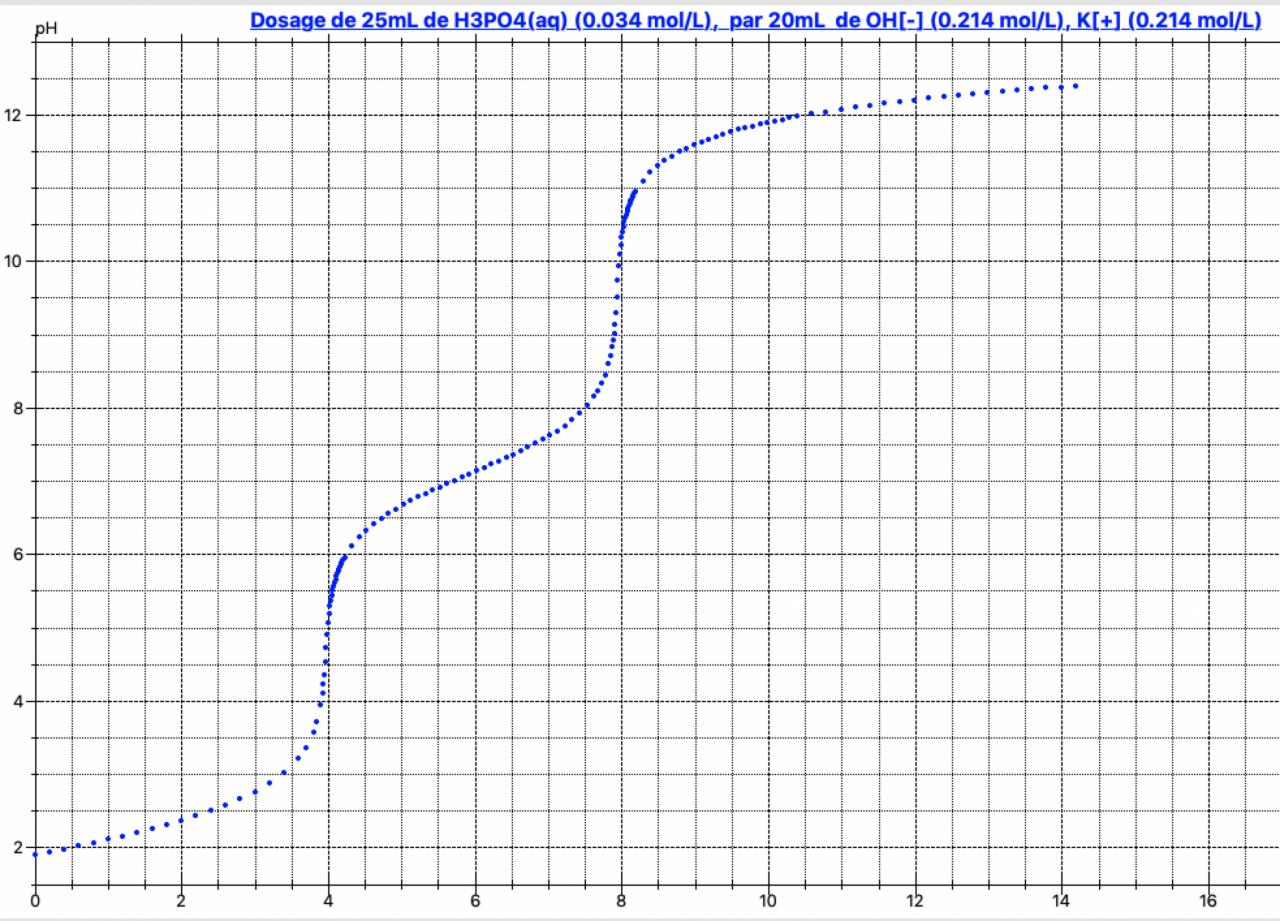
On dispose d'une solution de KOH contenant 3f dans 250ml. Pour neutraliser complètement 25ml de H3PO4, on utilise 12ml de KOH.
Quelle est la molarité de H3PO4 ?
J'ai donc calculé le nombre de moles de KOH avec n=m/M et j'ai obtenu 0,05moles... J'ai calculé la concentration de KOH avec C=n/V (en mettant tout en L) et j'ai eu 0,2 moles/L... Avec la formule C1V1=C2V2 j'ai obtenu une concentration molaire du KOH de 0,096 mol/L.... Je ne comprend pas pourquoi ce que j'ai fait est faux car la réponse est 0,034... Pouvez-vous m'aider s'il vous plaît ?
Merci d'avance
-----