Bonsoir
Ma question concerne les réactions de bromination sur le benzène (ou les composés aromatiques en général) :
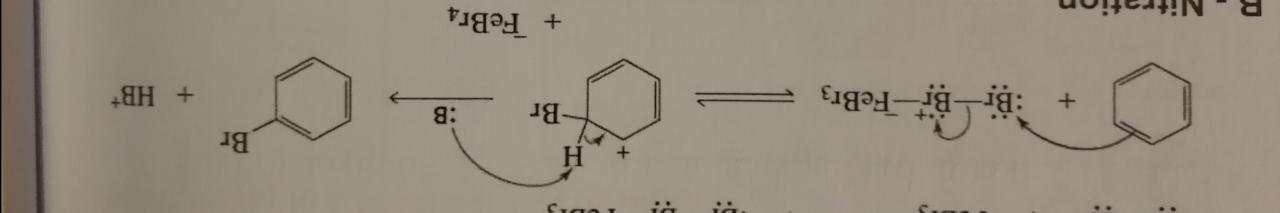
Le benzène a 3 doubles liaisons dont une qui va utiliser ses électrons pour attaquer l'atome Br chargé positivement d'une autre molécule (voir photo)
Je ne comprends pas comment le deuxième carbone de la double liaison peut perdre un électron et se charger positivement...
Pour moi la double liaison est faite grâce à 2 électrons pi qui viennent chacun d'un carbone engagé dans la double liaison. Et quand la double liaison attaque le Br je pensais qu'il n'y avait qu'un seul électron pi qui se reliait au brome, le deuxième carbone aurait donc récupéré son électron...
J'espère que ma question est assez claire... Je vous remercie pour vos réponse
Bonne soirée !
-----