Bonjour à tous,
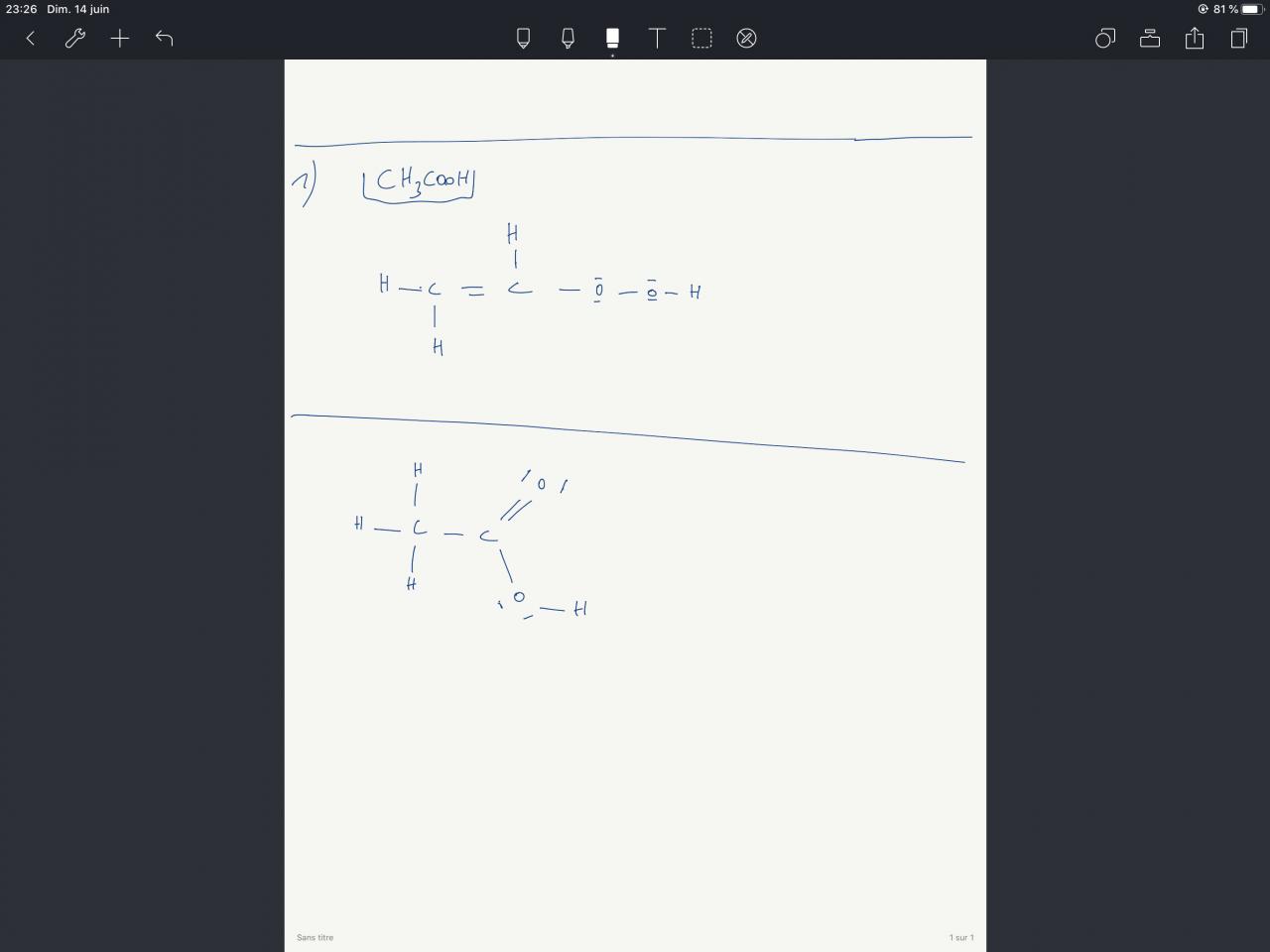
Je me retrouve face un dilemme, j'ai écris une fausse structure de Lewis pour le ch3cooh mais je n'arrives pas à voir mon erreur. J'ai bien sur comparé avec la bonne structure.
Dans ma structure la règle de l'octet est préservé ainsi que la charge formelle qui vaut bien 0 aussi ?
Une explication s'il vous plait ?
-----


