Bonjour, je suis actuellement bloqué sur mon exercice de chimie que je doit rendre demain,
Voici l'énoncé:
On dispose dune solution obtenue par dissolution dans leau dune base faible B. La constante dacidité K a
du couple A/B est connue. La concentration en base de la solution préparée est c.
On considère que la dissociation de leau est négligeable (pH> 7,5).
1. Après avoir établi léquation-bilan de dissolution de la base faible dans leau, exprimer la constante
d*équilibre de la réaction K. Etablir la relation qui la lie à Ka .
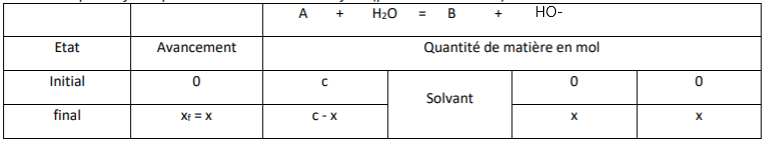
2. Etablir un tableau récapitulatif des nombres de moles des différents constituants à létat final en
raisonnant sur un litre de solution. On notera x la quantité dions OH- formés.
3. En déduire la relation entre le pH, le pKa et la concentration c pour une base faiblement dissociée.
4. Exprimer le pH dune base faible fortement dissociée.
Je bloque a la question 3, je ne vois pas comment trouver cette relation.
Merci d'avance de votre aide
-----