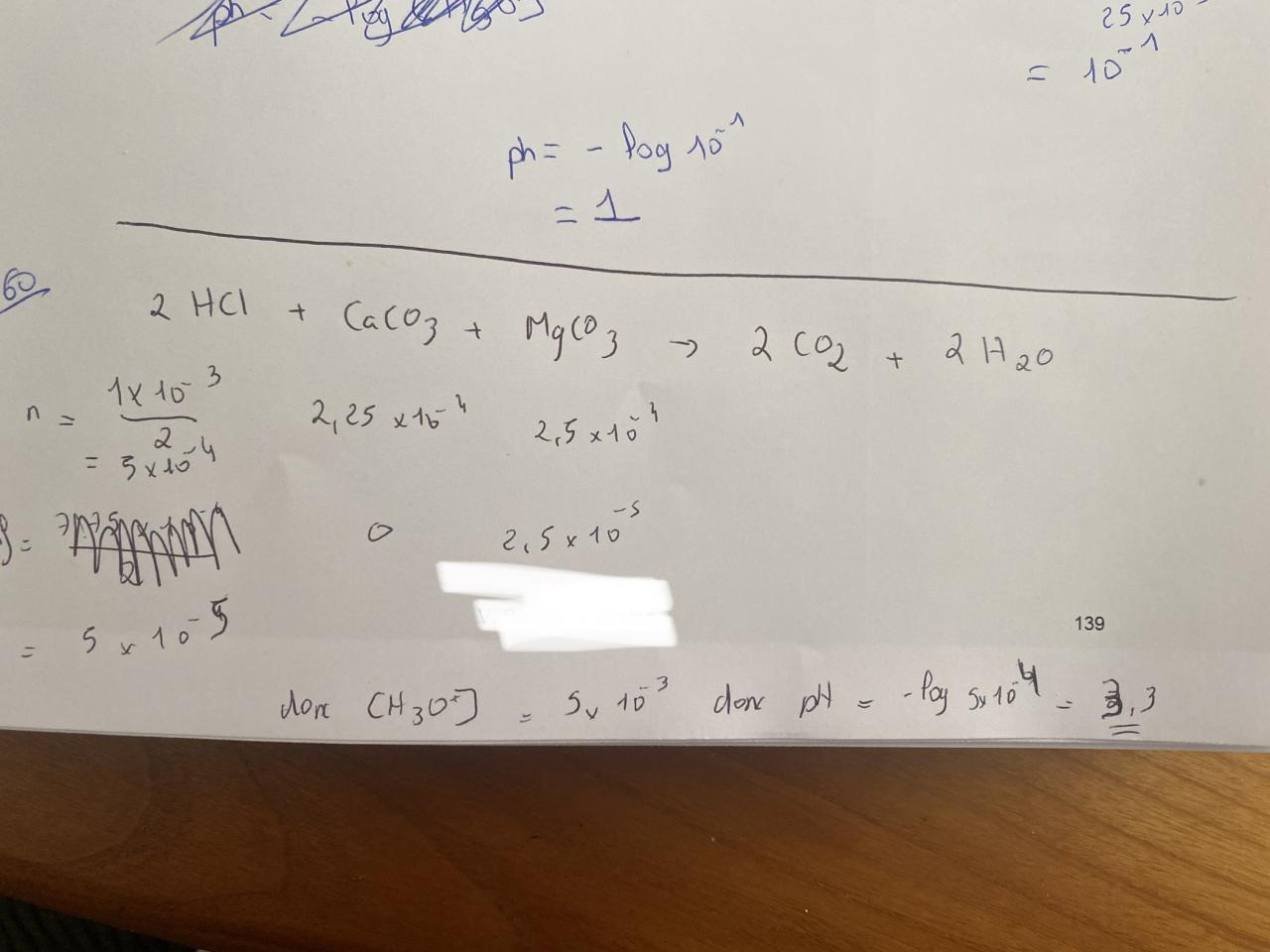Bonjour,
Je coince sur un exercice
Le suc gastrique est un acide très fort du à la présence d'acide chlorhydrique. Certains anti-acide aident à faire remonter le pH intra gastrique.
Un anti acide est composé de CaCO3 et MgCO3
A 100mL d'acide gastrique ayant un ph de 2,0, sont ajoutées 0,225 mmol de CaCo3 et 0,250 mmol de MgCo3.
Un gaz est formé. Quelle est la valeur du pH atteint à l'issue de cette réaction ?
Alors j'ai commencé par écrire l'équation en cherchant concentration H30+ ... mais je bloque complètement
Merci pour votre aide
-----