Bonjour,
J'ai une question qui est peut-être stupide, mais je suis entrain de faire des exercices sous format QCM en chimie organique, plus précisément sur les réactions des carbonyles. On doit trouver les réactifs d'une réaction en connaissait le produit de base et celui final avec quatre choix possibles et à nous de trouver la bonne. Le souci, c'est que j'arrive toujours à en garder 2, mais je n'arrive pas à les différentier, car la seule chose qui change, c'est que dans une réponse le réactif est en excès et dans l'autre en équi.
Je me demandais alors comment puis-je savoir si je dois prendre le réactif en équi ou en excès?
Et que s'il y a une "règle" pour cela, est-elle applicable aux autres réactions comme avec les alcanes, alcènes, .... ?
-----



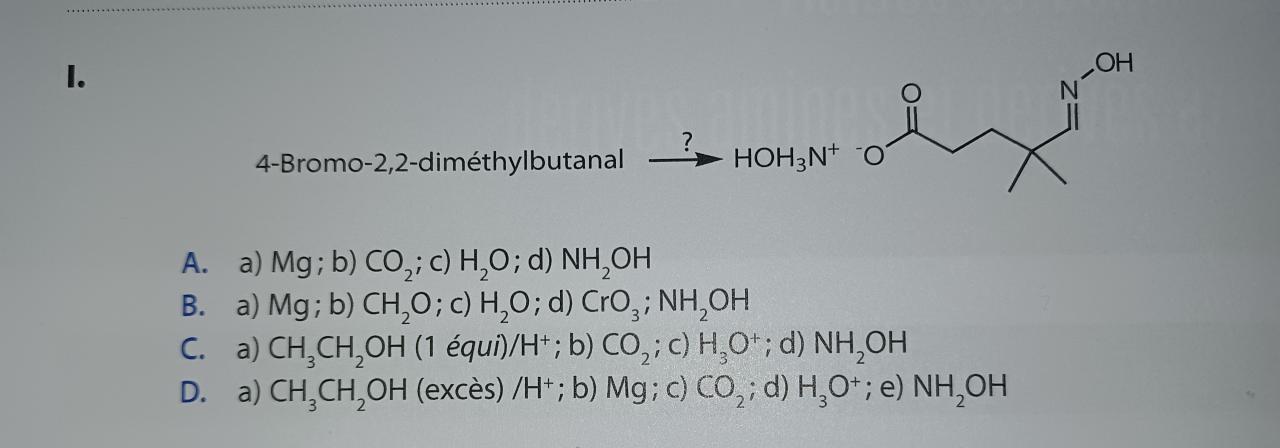
 ...)
...)