Bonjour à tous!
J'aurais encore une petite expérience a vous proposer:
Un expérimentateur souhaite quantifier précisément une quantité de production de gaz
dihydrogène et dioxygène par électrolyse de l'eau.
Il peut utiliser, entre autres, deux méthodes:
La méthode 'classique':
Connaissant la tension, l'intensité du courant et en fixant un temps précis d'électrolyse,
il peut en déduire combien de moles d'eau seront décomposées...
Cependant, la conductivité de l'eau pouvant varier au cours du temps ou érosion/corrosion des électrodes,
la régularité de la production peut être facilement faussée...
La méthode 'du condensateur':
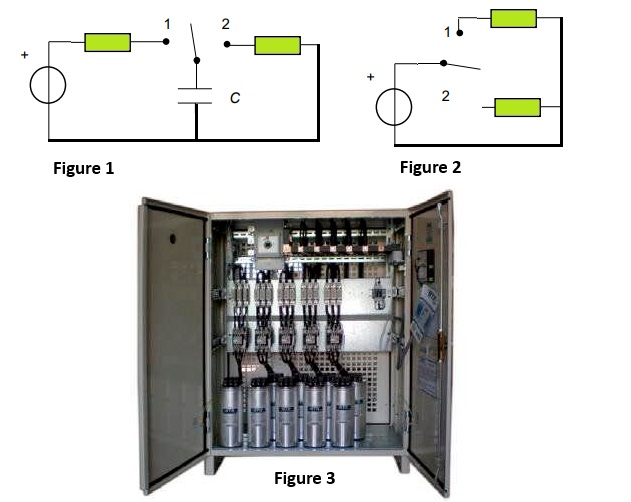
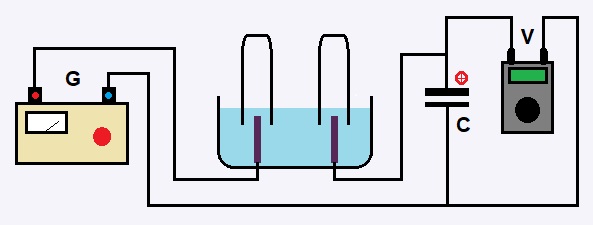
S'il souhaite plus de précision, il peut utiliser un condensateur
en créant le montage suivant:
Il lui suffit, alors et seulement, de disposer d'une alimentation a tension constante et de connaitre
la capacité du condensateur en Farad. Il n'a pratiquement même plus à se préoccuper du temps
que mettra lopération puisqu'une fois chargé, plus aucun courant ne circulera dans le circuit.
Au départ de l'expérience, le condensateur est complètement déchargé.
Une fois le condensateur chargé à une tension précise (ou à sa charge complète), l'expérimentateur sait exactement combien de
quantité d'électricité a traversé le montage et donc en déduire la quantité de gaz produit..
Qu'en pensez-vous?
-----




 )
)