Bonjour,
2 petites questions qui me tarodent :
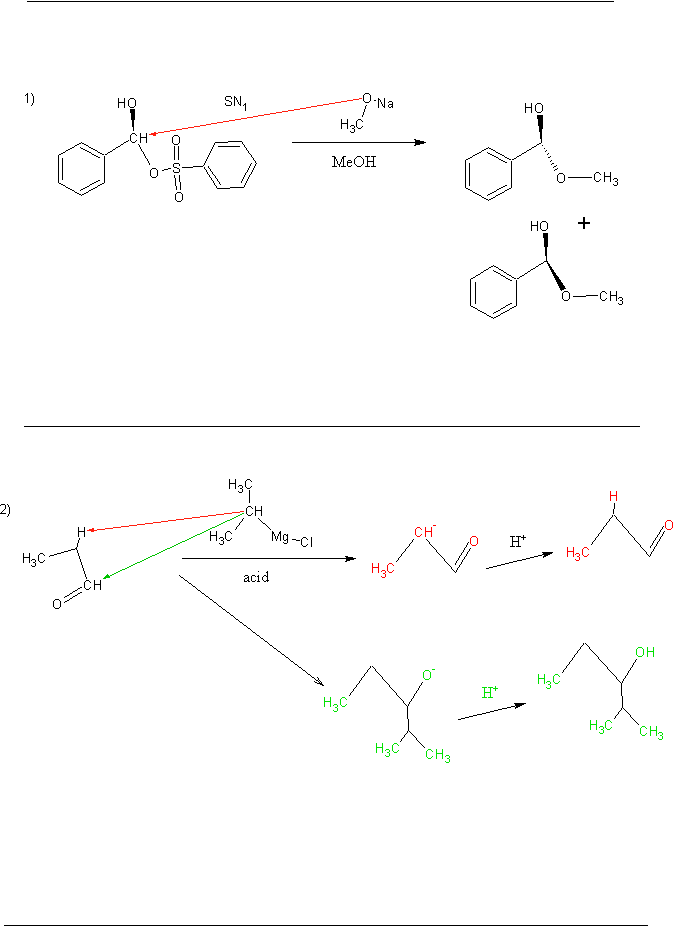
Sur la figure 1),
Est-ce que le MeO- attaque bien le carbone via une SN1 ( qui donne donc 2 enantiomères S et R ) ( ici c'est bien MeOh qui nous dit que c'est une SN1 ? ), ou MeO- attaque t-il le H de OH ?
Dans la figure 2 :
Il y a pour moi 2 type d'attaque possible, mais je n'arrive pas à déterminer laquelle est majoritaire
Merci d'avance pour votre aide !
-----