Bonjour à tous.
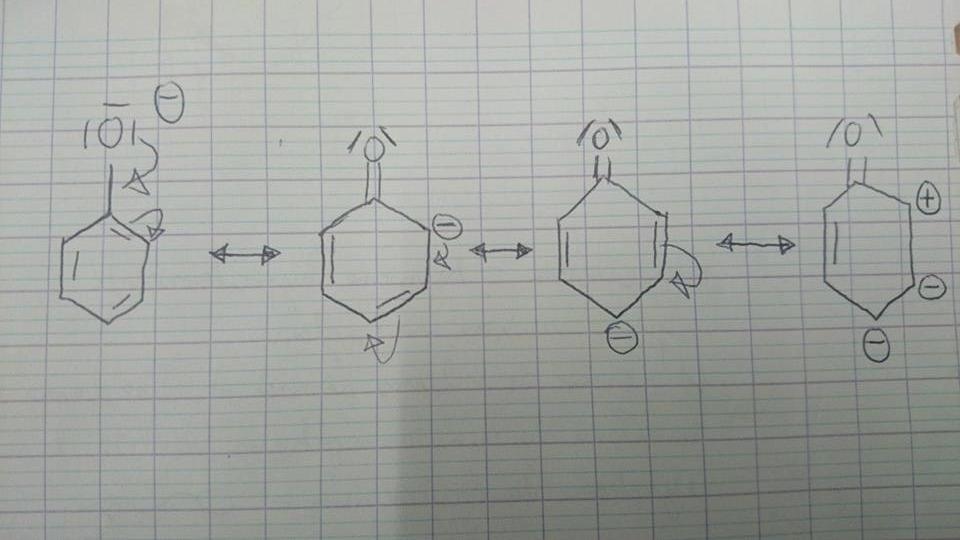
Je suis en première année de médecine à Pierre et Marie curie et je me demandais pourquoi lors de l'entrée d'une charge dans un cycle benzènique par mesomérie, (comme dans le cas du phenate par exemple) pourquoi la charge négative ne pouvait se retrouver en meta.
Merci à vous.
-----