Bonjour,
J'ai deux trois questions sur des choses auxquelles je ne vois pas d'explication (niveau PCSI), si vous avez des réponses ça serait parfait
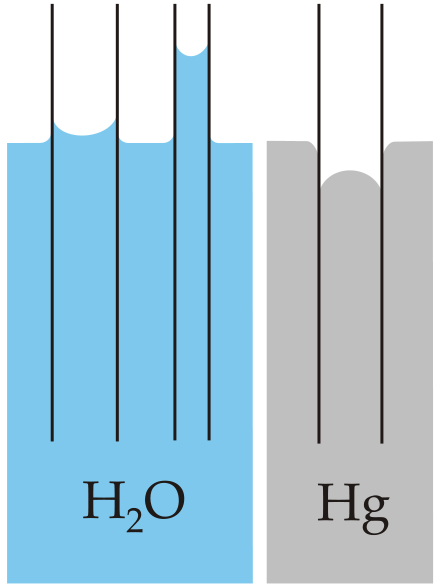
- D'abord, quand on fait une CCM, bon on place la plaque de CCM dans la cuve contenant l'éluant. Le solvant monte le long de la plaque par capillarité. Lorsqu'il arrive presque en haut de la plaque, on sort celle-ci de la cuve, on marque la ligne de front ... (source : mon TP d'il y a deux semaines). Il y a quelque chose que je ne comprends pas bien, comment ça se fait que le solvant monte par capillarité ; je suis allé voir sur wikipédia la page capillarité mais la seule chose que je comprends c'est ce phénomène :
Et ça n'explique pas trop pourquoi le solvant monte (ou alors je n'ai pas compris quelque chose, ce qui est certainement le cas)
- Autre chose que je n'ai pas compris (mais là il s'agit peut être d'une erreur du livre) : pour la Chromatographie sur colonne, il y a marqué pour le choix de l'adsorbant (pourquoi on ne dit pas absorbant d'ailleurs ?) : "De l'alumine neutre doit être utilisée pour purifier des alcools tertiaires qui pourraient se déshydrater sur une colonne de silice ou d'alumine acide". Alors, déjà pourquoi que les alcools tertiaires, ils ont tous dans tous les cas un groupe OH ? Et pourquoi ils pourraient se déshydrater sur quelque chose d'acide qui a tendance à céder un proton H+, pas à capter un proton H+ ? Ce serait pas plutôt sur une colonne d'alumine basique qu'il pourrait y avoir un problème entre le groupe OH de l'alcool et la base ? (Après mûre réflexion, je pense que le problème de mon incompréhension vient de "se déshydrater" mais je ne vois pas trop ...)
- Au niveau de la spectrophotométrie, choisir lambda max, j'ai compris que cela minimisait grandement l'incertitude, mais il y a une autre raison qui est décrite comme "augmentant la sensibilité, définie comme dA/dc maximale à lambda max". Je ne vois pas trop (pas du tout même) d'explications à ça :/
- Dernière petite question, mais je pense que la réponse est clairement non : on peut uniquement appliquer l'AEQS à un mécanisme en chaîne, on ne peut pas appliquer l'ECD ?
Merci beaucoup si vous avez des réponses, vous éclaireriez un pauvre petit sup !
-----