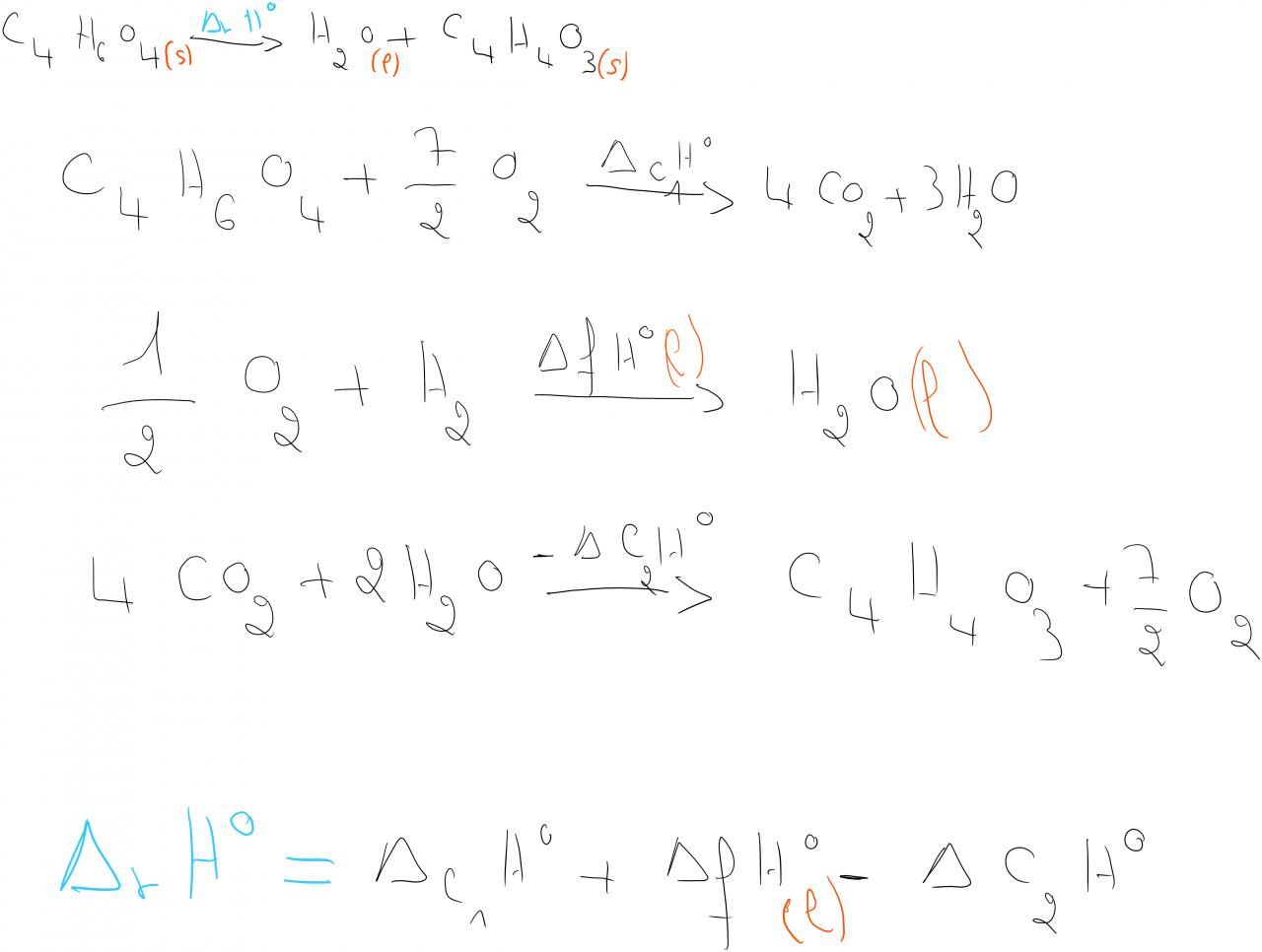Bonjour tout le monde,
Dans un exercice de thermo chimie, ils nous demandent de calculer la différence d'enthalpie de la réaction de déshydratation de l'acide succinique en son anhydre:
L'équation de la réaction est la suivante : C4H6O4 (s) ______> H2O(l) + C4H4O3(s),
On nous donne aussi : Delta C1 H°= energie de combustion de l'acide succinique
Delta C2 H°= energie de combustion de son anhydre
Delta f H° = energie de formation de H2O liquide
J'aimerai savoir si mon cycle est juste ou pas ?

Merci de votre aide !!
-----