Bonsoir,
j'aimerais connaitre le cheminement afin de répondre à cette question , le plus rapidement possible , car souvent je doute entre plusieurs items et je pers du temps pour le reste de mes question , si quelqu'un peut m'expliquer clairement comment faire , merci
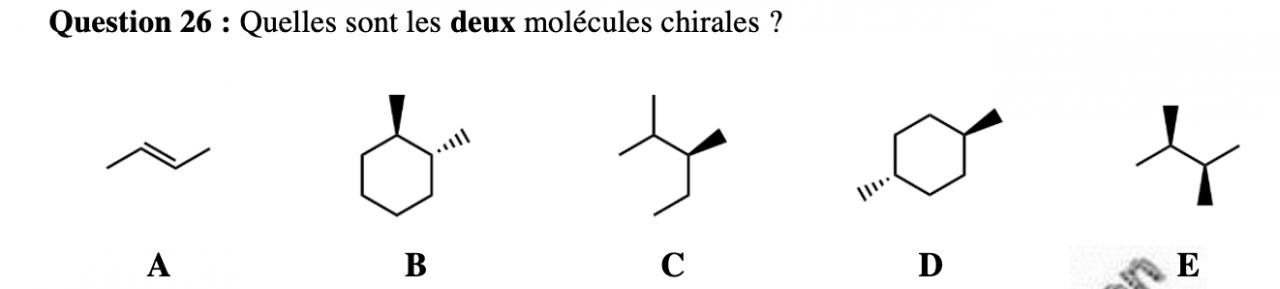
-----