Enoncé :
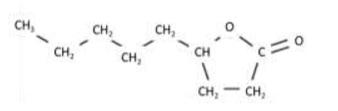
Pour former lester cyclique P (en image), les groupements fonctionnels hydroxy et carboxyle sont sur la même molécule de réactif. Ces deux groupements réagissent ensemble pour former lester cyclique.
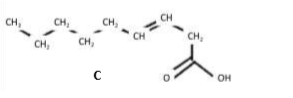
On me demande d'écrire la formule semi-développée de la molécule ouverte sachant que le composé polyfonctionnel contient un groupement hydroxy et un groupement carboxyle qui correspond au réactif avant cyclisation.
J'ai trouvé l'acide 4-hydroxynonanoïque.
Ensuite : Quelle autre molécule B de produit se forme au cours de la cyclisation ?
J'ai trouvé de l'eau mais je ne comprends pas pourquoi il faut séparer l'acide 4-hydroxynonanoïque de l'eau et par quelle méthode l'on pourrait le faire.
-----