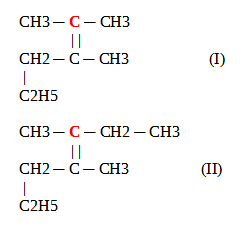Bonjour
je suis en premiere spé physique et j'ai cette molécule à nommer :
CH3 - CH2 CH3
| |
CH2 - C - CH3
|
C2H5
sauf que je comprends pas comment numéroter le C2H5, occupe t'il une seule place ou deux places du fait de la présence de deux carbones ?
merci !!
-----