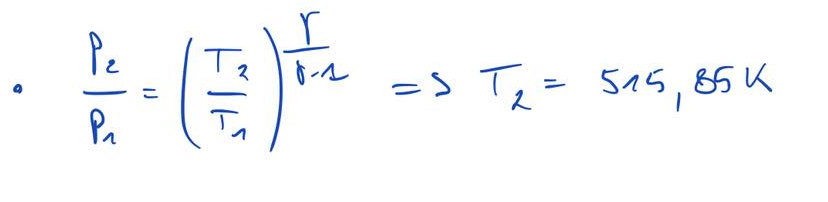Bonjour ! Je rencontre quelques difficultés pour la résolution de cet exercice de thermodynamique en système ouvert que voici :
De lhydrogène (gaz parfait aux propriétés constantes prises à température ambiante) est produità 30 bar et à température ambiante (300 K) via une électrolyse de leau. Afin de le stocker, on
souhaite augmenter sa pression à 200 bar. La compression se fait de manière isentropique dans un turbocompresseur (système ouvert). Le débit dhydrogène est de 100 g/s. Quelle sera la puissance du compresseur ?
A : 224 kW ; B : 22 kW ; C : 25 kW ; D: 314 kW ; E : 356 kW
Je suis parti de l'équation de Bernouilli en système ouvert en négligeant la différence d'énergie cinétique et potentielle et les travaux de frottements. J'ai donc une expression qui me dit : que le travail moteur est égal à l'intégrale de l'état 1 à 2 de vdp. Ce qui est équivalent à dire que : w_m = v (p2 - p1) [kJ/kg]
Est-ce correct ? Et si oui que puis-je faire pour en déduire la puissance du compresseur en kWatts [kJ/s]. J'ai essayé de multiplié par le débit qu'on donne dans l'énoncé ce qui me donne bien des Watts mais je n'arrive à aucune des réponses proposées...
Merci d'avance pour votre aide !
-----




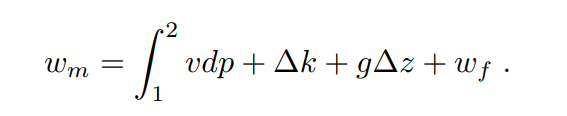
 ?
?