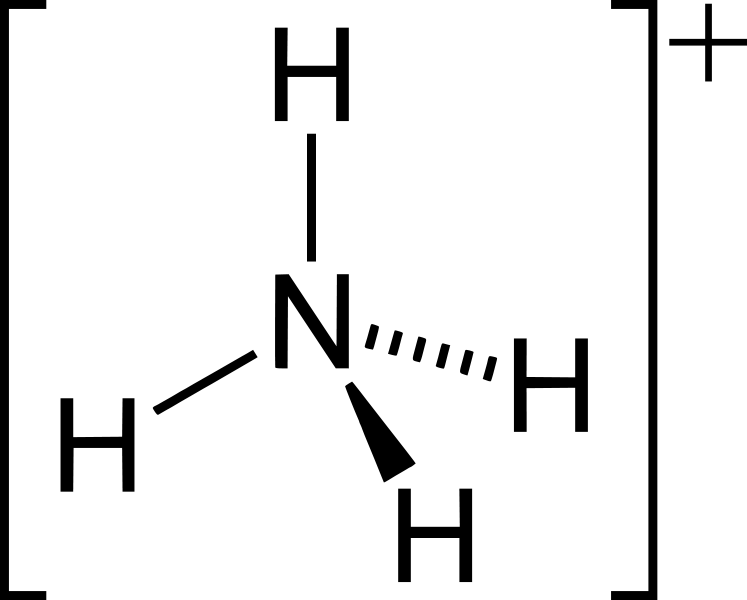
Bonjour, pour représenter NH4^+ avec la formule de lewis, j'ai un petit problème : H^+ a perdu un électron, il n'a donc aucun électron, il ne peut faire des liaisons que si N lui donne des électrons. Comme il y a 4H, donc N donnera 4 électrons et on aura donc écrit dans la formule de lewis, au milieu, :N^4+. Mais d'après la correction, il y a écrit N^+.
Merci.
-----





 A-B
A-B