Bonjour,
J'ai besoin de votre aide afin de comprendre les résultats que je trouve pour cet exercice.
Le tableau suivant donne els mesures de la vitesse initiale (en unités arbitraires) obtenures en l'absence et en présence de thréonine à une concentration de 40µmol/L. Ci dessous vous trouverez le tableau avec les données.
Je dois représenter les courbes vi=f([S]) en l'absence et en présence de thréonine et conclure (ci-dessous mes courbes)
J'envisage de conclure en disant : que la thréonine agit comme un inhibiteur de l'aspartikinase I en ralentissant la réaction enzymatique. elle régule négativement l'activité de l'aspartikinase I dans la voie de la biosynthèse des acides aminés.
Tableau des données.png
Cinétique a deux substrats et allosterie.xlsx
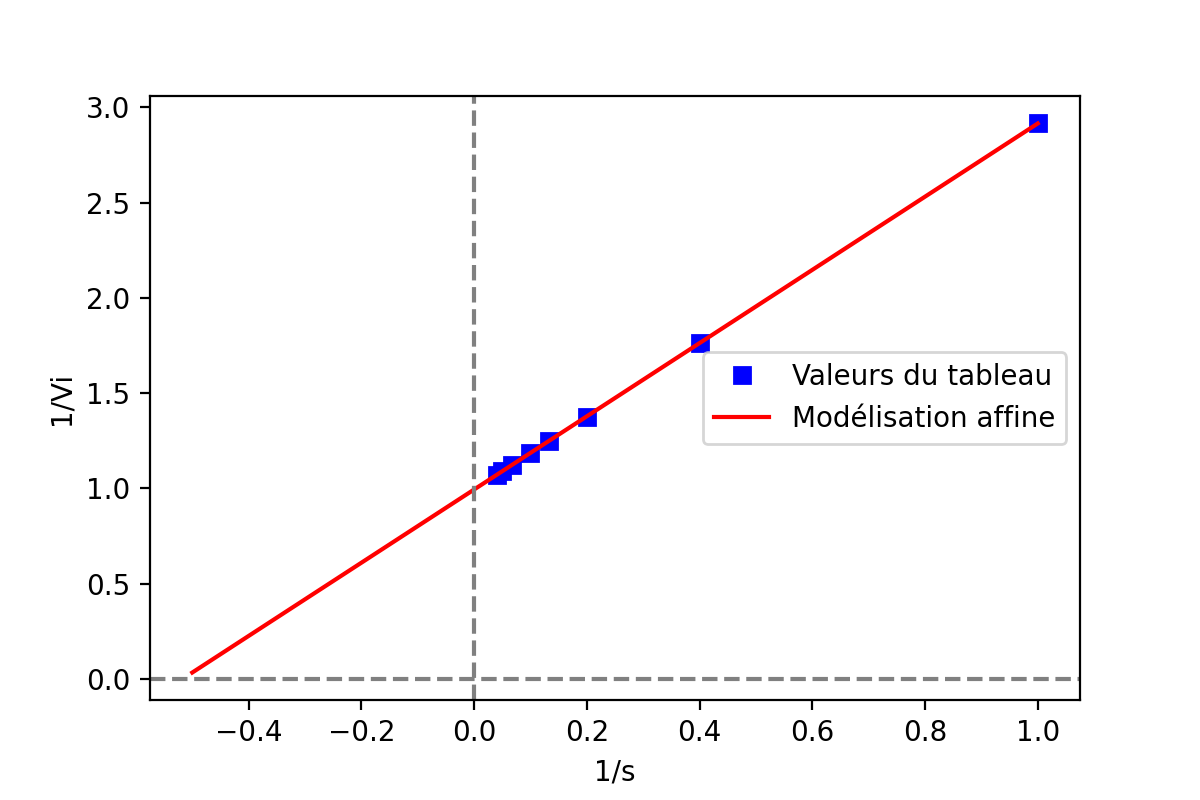
Je dois ensuite effectuer la représentation en double inverse en l'absence de thréonine voir graphique ci-dessus et je dois en déduire la constante de michaelis et celle de la vitesse maximale.
J'ai utilisé la droite d'équation étant donné que ma droite ne passe ni par l'axe des abscisses ni celle des ordonnées, je ne peux donc trouver graphiquement le Km et le Vmax.
J'ai considéré Y=aX+b et a= Km/Vmax 1000 Vi max /2 = 500 1/Vmax soit 1/500 =0,002 Vmax = 0,002 mol/L j'aurai pu prendre le b de mon équation plus juste soit 517,52
ensuite Km=520,53 x Vmax
km= 520,53 x 0,002= 1,041106 soit 1,04 mol/L
Pourriez-vous me donner SVP votre avis et m'apporter des explications si ma méthode est incorrecte?
Bon après-midi
-----




 et non
et non