Bonjour,
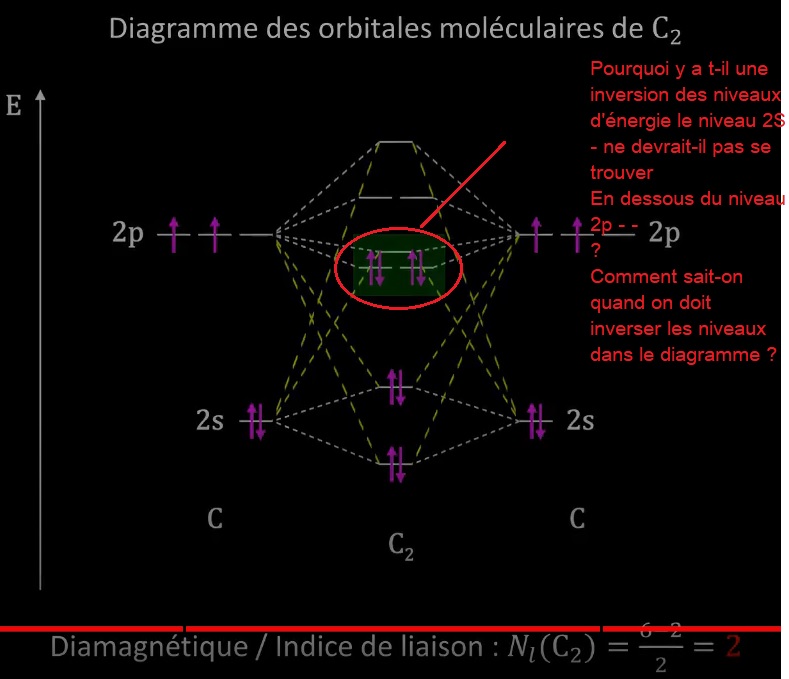
Je ne comprends pas pourquoi dans certains diagrammes, les niveaux d'énergie de la couche S et P sont parfois inversé, ce qui impacte généralement le résultat de OL
pour le type de liaison.
Comment sait-on qu'il faut faire cette inversion ? (Voir schémas ci-dessous dans le cercle rouge)
Le calcul de OL est simple une fois le diagramme effectué, mais pour les inversions de niveaux d'énergie cela semble plus compliqué...
Merci par avance pour vos éclaircissements.
-----


